De vergelijking van Arrhenius
Om een chemische reactie tot stand te brengen is een bepaalde hoeveelheid activeringsenergie nodig. De Zweedse scheikundige en Nobelprijswinnaar Svante Arrhenius heeft een vergelijking opgesteld die het verband aangeeft tussen het aantal reagerende moleculen, de temperatuur en de activeringsenergie:

![]()
Hierin is:
 de constante van Arrhenius;
de constante van Arrhenius; de activeringsenergie (in joule per mol);
de activeringsenergie (in joule per mol); de temperatuur (in kelvin);
de temperatuur (in kelvin); een getal dat aangeeft hoeveel moleculen er per seconde reageren.
een getal dat aangeeft hoeveel moleculen er per seconde reageren.
De vergelijking van Arrhenius kun je herleiden tot de volgende vorm:
![]()
Opdracht 11: (4 punten)
Geef een herleiding waaruit dit blijkt.
Aanpak:
In de vorm waar we naartoe moeten omschrijven staat de ![]() voor het
voor het ![]() -teken. Je krijgt dan ook de eerste drie punten voor het omschrijven van
-teken. Je krijgt dan ook de eerste drie punten voor het omschrijven van ![]() naar een vorm waar de
naar een vorm waar de ![]() alleen aan één kant van het
alleen aan één kant van het ![]() -teken staat. Dit doe je door bij iedere stap een variabele weg te werken aan de kant waar de
-teken staat. Dit doe je door bij iedere stap een variabele weg te werken aan de kant waar de ![]() staat.
staat.
Het laatste punt is dan voor de rechterkant om te schrijven naar de juiste vorm. Hiervoor moeten we de ![]() omschrijven naar
omschrijven naar ![]() . Dit doe je met behulp van de rekenregels
. Dit doe je met behulp van de rekenregels ![]() en
en ![]() .
.
Uitwerking met letters één voor één naar andere kant brengen:
Uitwerking met eerst 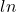 van beide kanten nemen:
van beide kanten nemen:
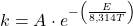 volgt
volgt




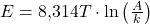
![]() en
en ![]() hebben voor elk soort reactie een eigen waarde. De waarden van
hebben voor elk soort reactie een eigen waarde. De waarden van ![]() en
en ![]() hangen niet af van de temperatuur. Omdat ze niet direct te meten zijn, meet men bij een reactie de waarde van
hangen niet af van de temperatuur. Omdat ze niet direct te meten zijn, meet men bij een reactie de waarde van ![]() bij twee verschillende temperaturen. Hieruit zijn dan met de vergelijking van Arrhenius de bij die reactie horende waarden van
bij twee verschillende temperaturen. Hieruit zijn dan met de vergelijking van Arrhenius de bij die reactie horende waarden van ![]() en
en ![]() te berekenen.
te berekenen.
Als voorbeeld bekijken we de chemische reactie waarbij stikstofdioxide wordt omgezet naar stikstofmonoxide en zuurstof.
Voor deze reactie is in een proef vastgesteld dat ![]() als
als ![]() en dat
en dat ![]() als
als ![]() .
.
Opdracht 12: (3 punten)
Bereken de waarde van ![]() van deze reactie. Geef je eindantwoord in de vorm
van deze reactie. Geef je eindantwoord in de vorm ![]() , met
, met ![]() afgerond op één decimaal.
afgerond op één decimaal.
Uitwerking:
- Invullen van
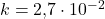 en
en 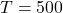 geeft
geeft 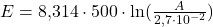
Invullen van en
en  geeft
geeft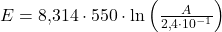
- Deze twee vergelijkingen samenvoegen geeft
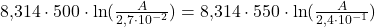 .
.
Voer in: .
. - Optie snijpunt geeft
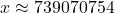 en
en 
Conclusie: De gevraagde waarde van is
is 